 市场资讯
市场资讯新闻资讯 更多+
(1)已上市药物情况:基因治疗药物全球商业化进程持续加快。截至2021年8月,全球共上市12款(FDA和EMA合计批准)基因治疗药物;2020年,全球基因治疗药物龙头诺华上市药物Zolgensma与Kymriah的合计销售额已达到14亿美元。
1)美国:截至2021年8月,美国FDA已批准的在售基因治疗药物有8个,其中5个CAR-T,2个病毒载体疗法,1个溶瘤病毒疗法。药物原研机构为科研院所的占比约50%。
美国食品药品监督管理局已批准的在售基因治疗制品分析
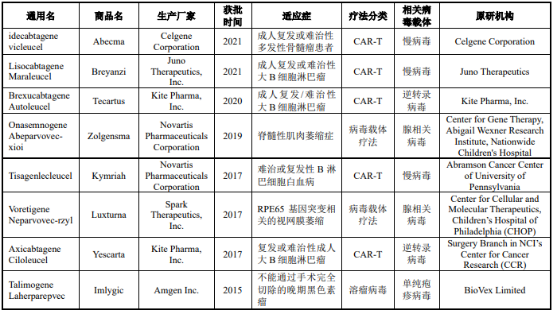
2)欧洲:截至2021年8月,欧洲药品管理局已批准的在售基因治疗药物有11个,其中3个是CAR-T疗法。药物原研机构为科研院所的占比约45.45%。
欧洲药品管理局已批准的在售基因治疗制品分析
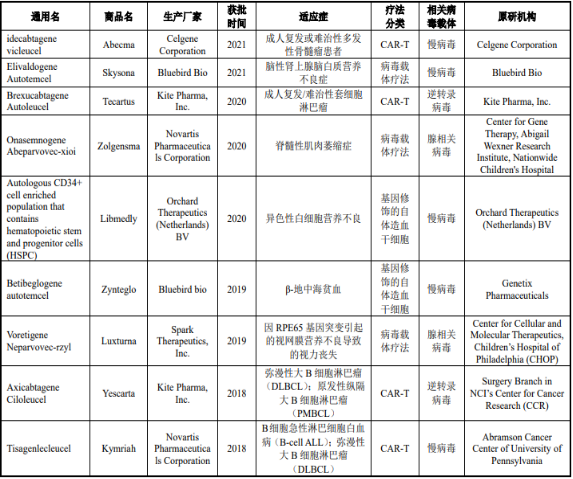
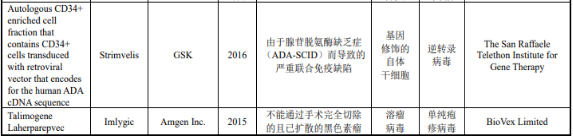
3)中国:截至2021年9月,除重组人5型腺病毒注射液(安柯瑞,Oncorine)之外,复星凯特的CAR-T产品——奕凯达®(阿基仑赛注射液)也于2021年6月23日获批,该药物系由复星凯特从美国KitePharma引进Yescarta技术,并获授权在中国进行本地化生产的靶向CD19自体CAR-T细胞治疗产品;药明巨诺的CAR-T产品——倍诺达®(瑞基仑赛注射液)已于2021年9月3日正式获批上市,这是中国第二款获批的CAR-T产品,也是中国首款1类生物制品的CAR-T产品。瑞基仑赛注射液是在美国Juno公司JCAR017基础上,由药明巨诺自主开发的靶向CD19的CAR-T产品。
中金企信国际咨询公布的《2022-2028年中国基因治疗药物市场运行格局及投资战略研究报告》
(2)临床试验情况:
1)在研临床试验数量:在技术、资本和政策的驱动下,全球基因治疗行业快速升温,大量基因治疗药物研发进入临床阶段,并自2015年起呈现爆发式增长。根据统计数据,截至2020年底,全球累计在研基因治疗临床试验超过1,300项。截至2020年底,美国是开展基因治疗临床试验数量最多的国家,累计超过650项;其次为中国,累计超过300项。
随着精准医疗的推进、基础研究和技术开发的进步、药物临床转化热度的提高,预计未来开展的基因治疗临床阶段试验将持续增加。
2)临床试验按治疗领域拆分:截至2020年12月,全球正在进行的基因治疗临床试验中,超过一半系针对肿瘤开发;此外,由于COVID-19新型冠状病毒的影响,2020年新增大量针对感染性疾病的基因治疗;其他适应症分布在血液系统疾病、内分泌系统和代谢性疾病、神经系统疾病、免疫系统疾病等领域。
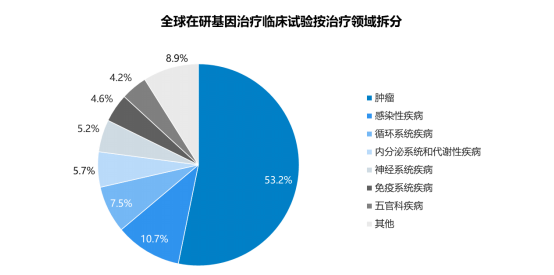
数据统计:中金企信国际咨询
截至2020年12月,国内在CDE注册的基因治疗临床试验中,针对肿瘤约占75%,针对感染性疾病和循环系统疾病各约占13%和11%。
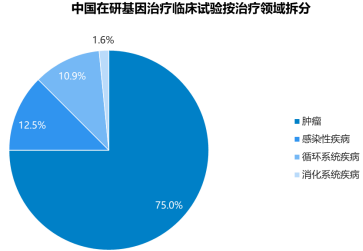
数据统计:中金企信国际咨询
3)基因治疗临床试验按阶段拆分:按基因治疗试验所处临床阶段,全球约39%临床试验处于临床I期,28%处于临床I-II期,25%处于临床II-III期,6%处于临床III期。
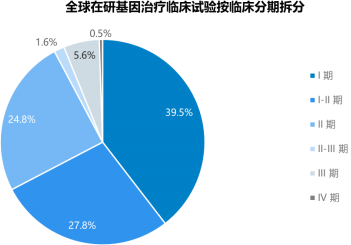
数据统计:中金企信国际咨询
国内在研基因治疗临床试验中,约52%处于临床I期,36%处于临床II期,13%处于临床III期。
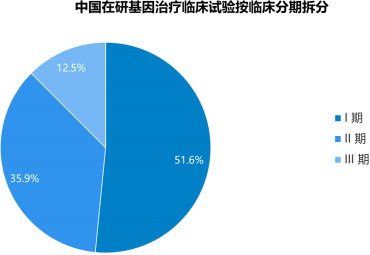
数据统计:中金企信国际咨询
(3)新药获批情况:截至2021年8月,FDA累计批准8款基因治疗产品,EMA累计批准11款基因治疗产品,近年来获批药物持续增加。预计到2025年,FDA每年将会批准10-20个基因治疗产品。总体上,基因治疗产业发展前景将长期向好。

 400-1050-986
400-1050-986

