 市场资讯
市场资讯新闻资讯 更多+
氯化氢(HCl)学名氢氯酸。是无色有刺激性气味的气体,空气中常以盐酸烟雾的形式存在。氯化氢的水溶液称盐酸,最高浓度可达43.4%;实验室常用浓盐酸的浓度为38%,相对密度1.19。含氯化氢20.24%的水溶液在110℃沸腾时组成不变,是共沸混合物。
|
分子式: |
HCl |
摩尔体积: |
22.25L |
|
分子量: |
36.46 |
液体比重: |
(10ºC,水=1):0.88 |
|
临界压力: |
8.258 Mpa |
1L液体(10ºC): |
540L气体(标升) |
|
临界温度: |
51.4 ºC |
1Kg液体(0ºC): |
613L气体(标升) |
|
临界密度: |
0.424g/cm |
溶解潜热: |
54.8Kj/Kg |
|
蒸发潜热: |
443.38Kj/Kg |
常压沸点: |
-85 ºC |
|
气体黏度(20ºC): |
1.56c/o 10-5Pa s |
定压比热(15ºC,0.1Mpa): |
Cp=0.812Kj/Kg K |
|
定容比热(15ºC,0.1Mpa): |
Cv=0.576Kj/ Kg K |
液体比重: |
(0 ºC,空气=1):1.268 |
|
气体密度: |
(0ºC 0.1Mpa ):1.639g/dm3 (21ºC 0.1Mpa ):1.522 g/dm3 |
||
液态氯化氢的蒸气压:
|
温度(ºC): |
-85.03 |
-10 |
0 |
10 |
20 |
30 |
40 |
|
压力(MPa): |
0.1 |
1.96 |
2.57 |
3.32 |
4.21 |
5.27 |
6.53 |
|
密度(g/cm3): |
1.191 |
0.962 |
0.924 |
0.881 |
0.831 |
0.772 |
0.697 |
氯化氢的物化特性:
①无色、有毒、刺激性、窒息性、不可燃气体;
②强吸湿性,吸收空气中的水分后,生成盐酸,具有强腐蚀性;
③比空气重,在湿空气中生产酸雾,强烈发烟;
④以液化气体形式储存于钢瓶中,压力(3-6Mpa)恒定,其职与气温有关;
⑤氯化锡、三氯化磷、溴化磷等无机化合物可溶于氯化氢中;
⑥石蜡、乙醇、乙醚、乙醛、酮、酸、酯、亚硝基、氰基等有机化合物能很好的溶解于氯化氢中,并可发生附加反应或脱水反应;
⑦纯液态氯化氢不与大多数金属发生反应,但与碱金属、铝、锰、铁、铜、锡、铅、锌等金属发生反应,并在其表面产生一层氯化物保护膜,当有水存在时,与金属发生反应,生成金属氯化物,并产生氢气。
(2)主要用途:目前,市场上化学级氯化氢产品主要用于医药中间体、农药及精细化学品制造业。电子级(VLSI)氯化氢产品主要用于半导体器件生产中单晶体硅片的清洗、气象抛光、外延基座腐蚀及硬质合金的制造。超纯氯化氢产品,主要用作标准物质和科学研究。
(3)产品包装:目前,国内大部分氯化氢产品采用HCL专用钢瓶包装,钢瓶符合国际GB5099-1994或DOT3AA标准,瓶阀为316L不锈钢隔膜式阀,接口为CGA330。
氯化氢主要生产技术路线:据中金企信国际咨询公布的《2020-2026年中国氯化氢市场竞争策略及投资可行性研究报告》统计数据显示:目前氯化氢主要工艺路线有:
(1)实验室制取氯化氢工艺:一般是用固体氯化钠和浓硫酸起反应,不加热或稍微加热,分别生成硫酸氢钠和氯化氢。

然后在500℃到600℃的条件下,继续起反应而生成氯化氢和硫酸钠。

总的化学方程式可以表示如下:

制备原理:高沸点(难挥发)酸制低沸点(易挥发)酸。
(2)工业制取氯化氢工艺:大规模的工业制造(氯碱工业)氯化氢方法是:通过电解食盐水得到烧碱的同时,可得到氯气和氢气。经过水分离后的氯气和氢气,通入合成炉进行燃烧生成氯化氢气体,经冷却后用水吸收制得盐酸成品,尾气经吸收后排空。

工业合成氯化氢原材料要求:
|
原料氢气 |
原料氯气 |
||
|
温度: |
40℃ |
温度: |
50℃ |
|
H2: |
98%(VOL%) |
Cl2: |
95%(VOL%) |
|
N2: |
2%(VOL%)(包括其他惰性气体) |
H2: |
0.4%(VOL%) |
|
H20: |
22.543%(Wt%) |
02: |
2.5%(VOL%) |
|
-- |
-- |
N2: |
2.1%(VOL%)
(包括其他惰性气体) |
|
-- |
-- |
H20: |
0.04%(Wt%) |
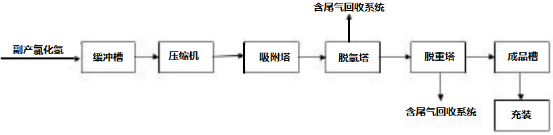
(3)副产物制取氯化氢/盐酸工艺:目前,工业领域如钢铁、石化、氯碱工业、有机氯化学、化工行业、电镀行业等领域的副产物都含有氯化氢。其中,国内成规模的有机氯化学品如异氰酸酯、甲烷氯化物、氯化石蜡、环氧氯丙烷和氯乙酸等产品副产氯化氢的量比较大(异氰酸酯副产的氯化氢占副产氯化氢总量的50%左右)。对于副产氯化氢气体,工业上主要通过压缩、吸附、精馏等工序制得高纯氯化氢产品,用于平板显示、光纤、集成电路等领域。
(1)生产路线对比:目前,实验室制取氯化氢工艺生产规模小,设备要求高,且氯化钠与浓硫酸产生的混合物较为坚硬,制取过程不方便。工业生产路线虽然可以大规模生产氯化氢,但对合成炉的要求较高。一般国内采用铁合成炉、“二合一”炉、“三合一”合成炉生产氯化氢。
(2)工业合成氯化氢(盐酸)过程合成炉的确定:
①铁合成炉制取氯化氢工艺的特点:铁合成炉制取盐酸的特点是本体不带冷却水套,氯、氢在铁合成炉内反应生成氯化氢,氯化氢气体直接和铁合成炉的内壁接触,造成对炉体氧化腐蚀较严重,导致铁离子进入氯化氢气体中,经吸收后制取的盐酸中含铁量偏高。颜色发黄,影响产品质量;铁合成炉因材质问题,易造成合成炉燃烧嘴腐蚀,燃烧嘴更换频繁;冷却盘管利用空气进行自然冷却,冷却盘管也易被腐蚀,容易形成三氯化铁堵塞空气冷却盘管及石墨冷却器入口,增加系统阻力,降低生产能力;由于反应过程放出大量的热量,在空气中自然冷却,合成炉周围的操作环境温度高。
②“二合一”合成炉制取氯化氢工艺的特点:氯气和氢气由合成炉的下部送入,采用向上燃烧方式。从合成炉顶出的氯化氢气体进入石墨冷却槽进一步冷却后,进入吸收塔吸收成合格盐酸送入盐酸储槽。
“二合一”炉是一种钢制石墨合成炉。合成炉的外壁采用钢板结构,内衬石墨,钢板和内壁之间是冷却水夹套。氯、氢2种气体在合成炉内反应时放出大量的反应热由炉体夹层冷却水吸收;氯化氢气体不与钢铁部分接触,无三氯化铁生成,生产的氯化氢质量提高;合成炉周围环境温度保持常温,操作入员的工作环境得到改善;装置的生产能力较过去大为提高:出合成炉的氯化氢气体采用钢制石墨冷却水冷却,和钢制冷却盘管相比冷却效果大大提高;“二合一”炉的热水废热可再次利用。
③“三合一”合成炉制取氯化氢工艺的特点:原料气体由合成炉的上部送入,燃烧方向为下向燃烧。生成的氯化氢气体立刻在下部的吸收段被水顺流吸收,成品盐酸由下部排出。未被吸收的氯化氢气体在尾部塔中进行逆流高效吸收,惰性气体等废气由水流泵抽出经处理后排空。
“三合一”合成炉是由燃烧喷嘴、燃烧室和降膜吸收塔构成的上下为一体的设备,盐酸制取的3个阶段(合成段、冷却段、吸收段)在1个设备内完成。燃烧喷嘴采用透明石英制的套管,向下安装在燃烧室最上部的不透性石墨支架内,内管通氢气气,外管通氯气。氯气和氢气在套管内混合燃烧,无论负荷大小火焰都能保持稳定。在合成段内外壁加工出环形或螺旋形强化传热槽,提高传热面积,有效地降低了氯化氢气体及合成段的温度;冷却段采用强化传热技术,在水夹套内增设导流板迫使冷却液成螺旋状围绕石墨炉筒外壁流动,提高流速;将水质点的运动由直线运动改为曲线运动,提高了水侧的传热效率,减缓了水垢的沉积,大大提高了合成炉的合成量,降低酸温和能耗;吸收段采用溢流管加外侧稳压环技术,使降膜吸收塔各吸收管内均有吸收液分布,提高了吸收效果和盐酸的单位产量,同时保障了盐酸的合格率。但是此合成炉结构复杂,不易清理结垢和检修。
总结:三种制取盐酸的合成炉都有各自的特点。铁合成炉由于生产过程中产生的大量热量直接在空气中冷却,造成操作环境温度高,盐酸产品中铁离子的含量高、质量低,已被许多的企业淘汰。
石墨“三合一”炉具有结构紧凑、传热效率高、拆装方便、使用寿命长、操作弹性强、盐酸质量好等优点,被广泛采用,但是此合成炉结构复杂,不易清理结垢和检修,由于其产量较小所以一般不用做大型氯化氢生产设备,而一般作为工业盐酸的生产设备。
“二合一”炉合成、冷却在炉体内完成,吸收在炉体外进行,其产量较大适合作为大型生产设备。而其既可以生产氯化氢气体,又可以部分吸收生产盐酸,可以满足不同的需要,具有更广阔的应用前景。

 400-1050-986
400-1050-986

