 研究报告
研究报告新闻资讯 更多+
对于国内而言,基因修饰动物模型行业属于新兴产业,应用前景广阔,增长潜力巨大;北美等发达地区是当前国际上最大的动物模型市场,但在新药研发、药物临床试验活动逐年增加的带动下,动物模型的使用需求仍保持了较高增速。总体上,我国动物模型服务行业的产业化发展尚不成熟,市场规模尚不具优势,但随着国内基础研究投入、医药研发投入和相关CRO服务规模迅速扩大,动物模型和基因修饰动物模型的重要性日益提高,市场规模将持续增长。
中金企信国际咨询公布的《2022-2028年中国基因修饰动物模型行业现状分析及赢利性研究预测报告》
(1)基因修饰动物模型的重要性:一方面,随着生命科学、医学的研究重心不断向基因功能研究转移,利用基因编辑技术和模式生物表型分析体系,从基因水平阐释人类基因组功能和人类疾病发病机制将是长期趋势。人类疾病发病与基因功能变化有强相关性,通过构建相关的基因修饰动物模型,将有效支撑疾病发病机制研究和诊疗手段的创新研发。比如,PD-1、PD-L1作为肿瘤治疗的靶点系通过对基因修饰小鼠的研究而发现,人源化小鼠模型也是相关抗肿瘤药物的有效筛选与评价工具。基因修饰动物模型在生命科学和医学中的作用将越来越突出。
另一方面,生物医药是我国现阶段及未来长期的重要战略性支柱产业。随着《“十三五”生物产业发展规划》、《“十三五”国家战略性新兴产业发展规划》等一系列利好政策出台,国内生物医药行业面临良好的发展机遇,相比成熟市场具有更大的发展空间,在全球基础研究、创新药研发、CRO服务领域中的地位将更加举足轻重。因此,基因修饰动物模型对于完善、夯实我国生物医药体系的重要性将不断提高,行业发展前景总体向好。
(2)基因修饰动物模型发展历程:
1)国内外情况比较:基因修饰动物模型服务行业系在实验动物行业的基础上发展而来。实验动物行业方面,欧美起步于20世纪初,国内起步于20世纪80年代初,发展时间相差约80年;基因修饰动物模型服务方面,国内外产业发展时间较为接近,但目前在行业关键、共性技术的自主研发能力,以及市场化成熟度和产业规模上还存在较大差距。CRISPR/Cas9和ES细胞打靶等共性、关键技术均源于欧美发达国家,国内企业的核心技术主要系基于对该等技术的应用、改良和创新,重大核心技术的原创能力不足。此外,国内行业规模整体较小,业内公司仍以服务科所院校为主,与大型医药企业、CRO公司的业务合作相对较少,市场成熟度与国外发达地区相比还存在较大差距。
但另一方面,我国凭借动物资源储备、科研人才储备、高学历人才优势,已逐渐成为包括全球知名药企和CRO公司的动物模型服务供应来源。且近年随着全球生物医药市场规模的持续扩张,动物实验模型的市场需求日益加大,发达国家受限于资源、成本等因素,依靠自身越来越难以满足对高品质动物模型的需求,因此在客观上为国内基因修饰动物模型服务行业提供了良好的发展机会。
2)行业发展里程碑:
①基因工程:基因工程的出现和进步是本行业的发展基础。作为一种使用生物技术直接操纵有机体基因组、改变细胞遗传物质的技术,基因工程通过分子克隆和DNA重组技术获得表达目标基因DNA序列,并通过导入到选定的宿主系统中,实现外源基因的表达,在生命科学和医学研究、工业和农业中均有广泛应用。在传统的生物医药工业领域,基因工程可用于大规模生产胰岛素、生长激素、干扰素、单克隆抗体、疫苗和众多其他药物;在基因治疗领域,基因工程技术将正常基因引入患者细胞内,通过原位修复有缺陷的基因,或替代缺陷基因的方式根治疾病,如Spark公司推出的以AAV为载体的基因治疗药物Luxturna,其可用于治疗因RPE65基因缺陷引起的视网膜疾病。在细胞治疗领域,采用基因工程的方法,对细胞进行工程改造,使之能在体内进行疾病的治疗,如目前已上市的诺华公司用于治疗复发或难治性急性淋巴细胞白血病的CAR-T细胞疗法Kymriah。
②基因修饰动物模型:1973年,鲁道夫·詹尼士通过引入外源DNA进入小鼠胚胎,创造了世界上第一个转基因动物,但基因无法传递到子代;1981年,FrankRuddle、FrankConstantini和ElizabethLacy的实验室将纯化DNA导入小鼠受精卵中,使转入的基因可以传递到小鼠的子代;1984年,携带癌基因可以用来诱发癌症的转基因小鼠成功构建;1989年,马里奥·卡佩奇、马丁·埃文斯和奥利弗·史密斯利用小鼠ES细胞打靶技术建立了第一个普通敲除小鼠模型并获得2007年诺贝尔生理学或医学奖。ES细胞打靶技术已被广泛应用于构建条件敲除、基因敲入、点突变、人源化等模型。
③基因编辑技术:基因编辑技术目前已经发展到第三代。
第一代技术:1996年锌指核酸酶技术(ZFN)的建立使人工定点诱导双链DNA断裂成为现实,实现了基因编辑技术里程碑式的突破。锌指核酸酶,由锌指蛋白(ZFP)和FokⅠ内切酶的核酸酶结构域组成,前者负责识别DNA位点,后者负责切割DNA。ZFN从2001年开始被陆续用于不同物种的基因编辑,在用于构建基因编辑模式生物的同时,也被应用于遗传育种和基因治疗,但编程性差、制作繁琐、效率较低。
第二代技术:转录激活效应因子核酸酶(TALEN)技术。TALEN的构造与ZFN类似,由TALE基序串联成决定靶向性的DNA识别模块,与FokⅠ核酸酶结构域连接而成。与ZFN技术相比,TALEN技术大大提高了编程性能,设计简单,因此自2011年建立后迅速应用于构建基因修饰动物模型、遗传育种和基因治疗等领域,并入选为2012年的《科学》(Science)的年度十大科技突破之一。
第三代技术:CRISPR/Cas系统介导的基因编辑技术。CRISPR/Cas系统是细菌和古细菌中进化出来用于抵御噬菌体及外源DNA入侵的适应性免疫系统,2012年其详细机制被发现。与ZFN和TALEN技术相比,CRISPR/Cas技术的设计和制备更加简单,成本更低,编辑效率更高,并衍生出多种基因编辑系统,是目前最重要、最主流的基因编辑技术之一。CRISPR/Cas9连续多年被《Nature》评为最有前景的技术之一,在2015年被《Science》评为技术突破第一名,在2014年和2016年被《麻省理工科技评论》评为10项突破技术之一,2020年诺贝尔化学奖颁给了CRISPR/Cas9的发现者。
(3)基因修饰动物模型服务行业技术:本行业的主要技术为基因修饰类技术和胚胎工程技术。
1)基因修饰类技术:
①基于CRISPR/Cas系统的基因修饰技术,简称CRISPR/Cas技术:CRISPR/Cas系统是细菌和古细菌在长期演化过程中形成的一种适应性免疫防御机制,用来对抗入侵的病毒及外源DNA。CRISPR/Cas系统可以在真核细胞中高效发挥DNA编辑作用,针对基因组特定位点造成DNA双链断裂。DNA双链断裂后,可发生非同源末端连接,修复断裂DNA,造成小片段碱基的插入或缺失;也可以发生同源重组介导的DNA修复,该过程可在断裂位点引入操作者提供的修复DNA模板,从而达到外源DNA片段敲入或内源DNA片段替换的效果。
利用CRISPR/Cas获得基因修饰动物模型的主要技术路线为:1)针对基因组特定序列设计向导RNA(gRNA);2)将gRNA、Cas蛋白或者mRNA以及修复模板注射到小鼠受精卵中,获得F0代小鼠;3)对F0代小鼠进行基因型鉴定,筛选获得阳性F0代小鼠,通过与野生型小鼠交配获得基因编辑F1代杂合子小鼠。简要流程示意图如下:

②基于ES细胞打靶的同源重组技术,简称ES细胞打靶技术:小鼠胚胎干细胞(ES细胞)具有发育全能性,能够分化为各种类型的细胞,可在体外培养扩增并保持发育的全能性。基因同源重组是指当外源DNA片段与宿主基因组片段序列相同或相近,两者互补结合时,结合区的任何部分都有与宿主的相应片段发生交换(即重组)的可能,这种重组称为同源重组。基于小鼠胚胎干细胞的同源重组技术,是在小鼠胚胎干细胞内通过同源重组对目的基因进行修饰和替换,然后将基因修饰后的ES细胞注射到小鼠囊胚中,并移植到代孕母鼠中发育成基因修饰小鼠的技术。
基于小鼠胚胎干细胞的同源重组基因修饰技术流程如下图所示:根据基因修饰要求,构建同源重组打靶载体;将该打靶载体转入ES细胞中,并通过药物筛选获得ES细胞抗性克隆;将同源重组阳性的ES细胞克隆显微注射到囊胚中,获得嵌合体小鼠(F0代小鼠);嵌合体小鼠和野生型小鼠交配后获得基因修饰的F1代小鼠。
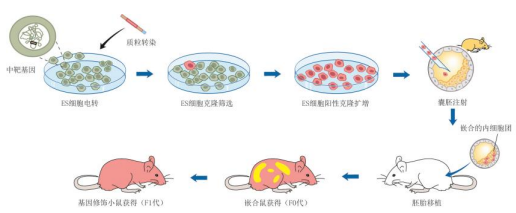
2)胚胎工程技术:胚胎工程技术是指对早期胚胎或配子所进行的操作和处理技术,包括体外受精、受精卵显微注射、囊胚注射、单精注射、胚胎移植、胚胎冻存复苏等技术。这些技术可以帮助人们在体外条件下实现动物受精和早期胚胎发育,完成动物的基因编辑,开展品系的保存延续和种群扩繁等工作。
①体外受精技术:体外受精技术(Invitrofertilization,IVF),是指通过卵子与精子在体外条件下人工受精,培养发育为早期胚胎后,再通过胚胎移植技术将发育的胚胎植入代孕母鼠子宫内,使其发育成子代小鼠的技术。该技术利用超排激素刺激雌鼠超排卵,可以在极少量雄鼠的条件下,一次性获得成百上千只同日龄的子代小鼠,节省繁育的时间和成本。
②单精注射技术:单精注射技术,全称:单精子显微注射技术(Intracytoplasmicsperminjection,ICSI),是指通过显微操作系统将单个精子头注入小鼠卵子胞浆内,使卵子受精并发育成小鼠的技术。该技术精简了受精过程,可以用于挽救因为精子无活力或者活力低造成雄性不育的小鼠品系。
③精子、胚胎冻存复苏技术:精子或者胚胎冻存技术是指将小鼠的精子或者胚胎放在特殊的冻存液中,通过程序降温或者快速冷冻的方法,将精子或者胚胎储存于液氮中,用于品系的长期保存;胚胎复苏技术是指通过升温的办法将冻存的精子或者胚胎解冻,将存活的胚胎移植到代孕小鼠子宫内发育,进而获得冻存品系小鼠活体的技术。
(4)基因修饰动物模型产业链:
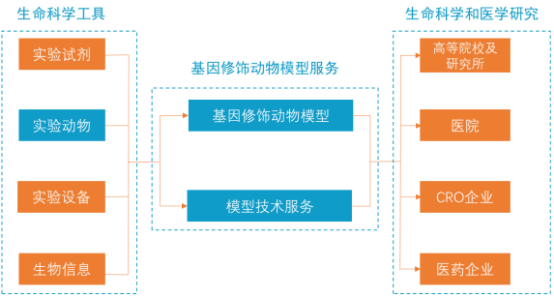
基因修饰动物模型行业上游为生命科学工具行业,包括实验动物、实验设备、实验试剂、生物信息等领域;下游为生命科学和医学研究行业,包括科所院校、医药公司、CRO公司等研发活动实施主体。
1)生命科学工具:生命科学工具一般包括实验试剂、实验动物、实验设备和生物信息。其中,实验试剂主要指用于反应、培养、标记、检测等用途的各类分子、生化试剂和细胞试剂等;实验设备主要是指测试仪器、分析设备、动物饲养笼具等;生物信息主要是指基因的序列信息;实验动物主要指用于疾病模拟、药效试验、毒理分析等由国家法律规定的物种,如小鼠、大鼠、犬类、猴子等。模式生物的涵盖面更大,包括实验动物,也包括尚未列入实验动物的其它研究用物种,如果蝇、线虫、斑马鱼等。
(5)生命科学和医药研究投入规模:生命科学和医学研究大行业研发投入主要来自生命科学研究、药物研发、CRO服务等细分领域。
1)我国整体R&D经费投入情况:根据国家统计局《全国科技经费投入统计公报》等资料,2019年全国投入R&D经费22,143.6亿元,同比增长12.5%;其中,基础研究、应用研究和试验发展的经费投入分别为1,335.6亿元、2,498.5亿元和18,309.5亿元,分别同比增长22.5%,14.0%和11.7%,并呈现如下特点:
①基础研究经费快速增长。2018年,基础研究投入首次突破千亿元大关;2019年,基础研究占R&D经费比例首次突破6%。高等学校、政府所属研究机构和企业的基础研究经费分别为722.2亿元、510.3亿元和50.8亿元,前两者合计占比92.28%,是我国基础研究经费投入的主要来源。
②国内R&D规模和结构的优化空间较大。总体上,我国R&D经费投入规模总体增长较快,但主要来自应用研究的经费增长,基础研究投入较低,与欧美发达国家的差距较大;R&D规模方面,虽然总量自2013年起已稳居世界第二,R&D投资强度在2019年达到2.23%,但与美国、日本的投资强度相比仍有差距。因此,我国R&D经费在规模和结构上仍有较大优化空间。
2)生命科学研究投入情况:欧美发达国家是目前全球生命科学研究经费投入的主要来源,也是各类动物模型的主要消耗国家。以美国国立卫生研究院NIH为例,根据德勤《2020全球生命科学行业展望》,2013年至2018年,NIH从联邦政府获得的资金从293亿美元增至373亿美元,CAGR达到4.95%。2019年全年预算达到392亿美元,延续了上升趋势。相较于欧美发达国家,国内生命科学研究起步较晚,研发能力偏弱,研究支出占全球总体份额不高,但随着国家在基础科研建设上的不断重视和发力,近5年来,国家主要科技计划在生命科学领域的累计投入约600亿元,在干细胞、合成生物学、神经生物学、纳米生物等多个领域实现了突破。预计未来几年,生命科学领域的投入规模将继续增长。

 400-1050-986
400-1050-986

